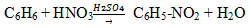- Плотность бензола
- Плотность бензола и другие его физические свойства
- Химический состав и строение молекулы бензола
- Краткое описание химических свойств и плотность бензола
- Примеры решения задач
- Плотность бензола и толуола при различных температурах
- Теплопроводность, плотность и свойства пара бензола
- Свойства пара бензола
- Теплопроводность пара бензола
- Таблица давления насыщенного пара бензола.
- Теплопроводность, плотность и свойства пара бензола
- Свойства пара бензола
- Теплопроводность пара бензола
- Таблица давления насыщенного пара бензола.
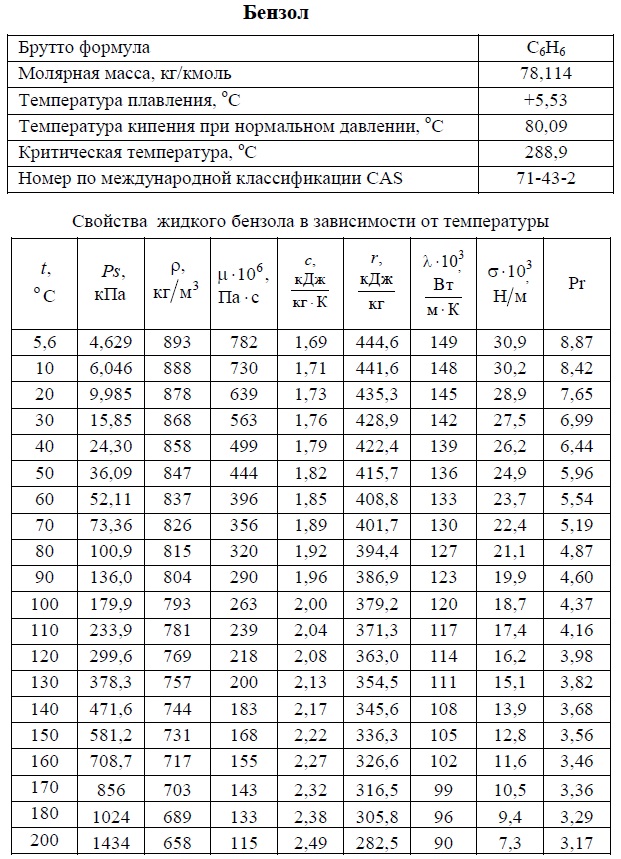
- Бензол — свойства. T: +5,6/+200°C. Температуры кипения, плавления, критическая, молярная масса, плотность, вязкость, теплоемкость, теплота парообразования, теплопроводность, число Прандтля, коэффициент объемного расширения
- Бензол — свойства. T: +5,6/+200°C. Температуры кипения, плавления, критическая, молярная масса, плотность, вязкость, теплоемкость, теплота парообразования, теплопроводность, число Прандтля, коэффициент объемного расширения.
- Бензол — свойства. T: +5,6/+200°C. Температуры кипения, плавления, критическая, молярная масса, давление насыщенных паров, плотность, вязкость динамическая, теплоемкость, удельная теплота парообразования, теплопроводность, число Прандтля, коэффициент объемного расширения. Таблица.
Плотность бензола
Плотность бензола и другие его физические свойства
Основные физические константы бензола приведены в табл. 1. Он широко используется в промышленной органической химии в качестве растворителя и сырья для синтеза красителей, полимеров, взрывчатых веществ, поверхносто-активных веществ, лекарственных препаратов. Бензол растворяет жиры, полимеры, нефтепродукты, масла, лаки.
Таблица 1. Физические свойства и плотность бензола.
Температура плавления, o С
Температура самовоспламенения, o С
Динамическая вязкость, Па×с
Бензол токсичен, вдыхание его паров вызывает острое отравление, приступы головокружения, судороги. При хроническом отравлении бензол поражает почки, печень, костный мозг, приводит к уменьшению в крови эритроцитов.
Химический состав и строение молекулы бензола
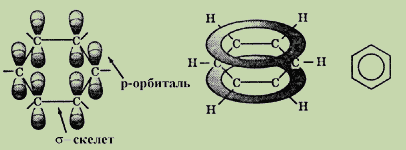
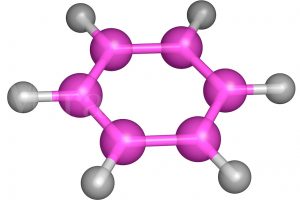
Химический состав молекулы бензола можно отразить при помощи эмпирической формулы C6H6. Согласно представлениям современной органической химии, молекула бензола является правильным плоским шестиугольником. Все шесть атомов углерода находятся в sp 2 -гибридном состоянии. Каждый атом углерода образует σ – связи с двумя атомами углерода и одним атомов водороды, лежащими в плоскости цикла. Валентные углы между тремя σ – связями равны 120 0 .
Каждый атом углерода в молекуле бензола имеет одну негибридизованнуюp – орбиталь. Шесть этих орбиталей располагаются перпендикулярно плоскому σ – скелету и параллельно друг другу. При их взаимном перекрывании образуется единое π-электронное облако, т.е. осуществляется круговая делокализация электронов. Наибольшая π-электронная плотность в этой сопряженной системе располагается над плоскостью σ – скелета молекулы и охватывает все шесть атомов углеродного цикла. В результате все связи между атомами углерода в бензоле выравнены и имеют длину 0,139 нм (рис. 2).
Рис. 2. Строение молекулы бензола.
Краткое описание химических свойств и плотность бензола
Для бензола характерны реакции замещения, протекающие по электрофильному механизму:
— галогенирование (бензол взаимодействует с хлором и бромом в присутствии катализаторов – безводных AlCl3, FeCl3, AlBr3)
— нитрование (бензол легко реагирует с нитрующей смесью – смесь концентрированных азотной и серной кислот)
— алкилирование по Фридею-Крафтсу
Реакции присоединения к бензолу приводят к разрушению ароматической системы и протекают только в жестких условиях:
— гидрирование (реакция протекает при нагревании, катализатор – Pt)
— присоединение хлора (протекает под действием УФ-излучения с образованием твердого продукта – гексахлорциклогексана (гексахлорана) – C6H6Cl6)
Примеры решения задач
| Задание | Вычислите плотность а) по кислороду; б) по азоту; в) по воздуху следующих газов: пропана C3H8 и стибина SbH3. |
| Решение | Для того, чтобы вычислить относительную плотность одного газа по другому, надо относительную молекулярную массу первого газа разделить на относительную молекулярную массу второго газа. |
Относительную молекулярную массу воздуха принимают равной 29 (с учетом содержания в воздухе азота, кислорода и других газов). Следует отметить, что понятие «относительная молекулярная масса воздуха» употребляется условно, так как воздух – это смесь газов.
| Задание | Плотность некоторого газа по гелию составляет 10. Известно, что газ является простым веществом. О каком веществе идет речь? |
| Решение | Отношение массы данного газа к массе другого газа, взятого в том же объеме, при той же температуре и том же давлении, называется относительной плотностью первого газа по второму. Данная величина показывает, во сколько раз первый газ тяжелее или легче второго газа. |
Молярная масса газа равна его плотности по отношению к другому газу, умноженной на молярную массу второго газа:
Тогда, молярная масса газа будет равна:
Среди простых веществ в газообразном состоянии находятся азот, кислород, водород, хлор, неон, гелий, фтор, аргон, криптон, ксенон и радон.
Формула молекулы аргона Ar. Относительная атомная масса аргона равна 39,948 а.е.м. Значит искомый газ – это аргон.
Плотность бензола и толуола при различных температурах
Приведены таблицы значений плотности бензола C6H6 и толуола C7H8 при различных температурах. Плотность в таблицах дана для жидкого состояния этих веществ в размерности кг/м 3 .
Бензол и толуол относятся к ненасыщенным ароматическим углеводородам (гомологический ряд CnH2n−6) и при нормальных условиях представляют собой жидкости легче воды с резким специфическим запахом.
Молярная масса бензола составляет 78,11 г/моль, толуола — 92,13 г/моль. Бензол является более тяжелой жидкостью — его плотность при 20 градусах Цельсия выше плотности толуола на 14%.
При нормальном атмосферном давлении бензол существует в виде жидкости при температурах от 5,5°С. Его температура кипения составляет 80,1°С. Выше температуры кипения плотность бензола приведена в таблице при давлении, превышающем 760 мм. рт. ст.
Плотность бензола при 20°С составляет величину 879 кг/м 3 и при нагревании снижается. При температуре кипения она становится равной 815 кг/м 3 . Образующиеся в процессе кипения пары бензола имеют плотность 2,69 кг/м 3 .
| Температура, °С | Плотность бензола, кг/м 3 | Температура, °С | Плотность бензола, кг/м 3 |
|---|---|---|---|
| 7 | 910 | 80 | 815 |
| 20 | 879 | 90 | 804 |
| 30 | 869 | 100 | 793 |
| 40 | 858 | 120 | 769 |
| 50 | 847 | 130 | 757 |
| 60 | 836 | 140 | 745 |
| 70 | 826 | 150 | 733 |
Толуол в жидком виде (при нормальном атмосферном давлении) существует лишь в интервале температуры выше -95°С и закипает при 110,6°С. Значения плотности жидкого толуола даны в таблице в более широком диапазоне: от -90 до 150°С.
Плотность толуола при 20°С имеет значение 867 кг/м 3 . При росте температуры толуол, как и бензол, расширяется и становится менее плотным. Например, при температуре 100°С его плотность снижается до величины 790 кг/м 3 .
Следует отметить, что при температуре 150 градусов плотность толуола становится равной этому показателю у бензола и составляет 733 кг/м 3 . Кроме того, при дальнейшем нагреве толуола выше температуры 320°С достигается его минимальная (критическая) плотность, равная 290 кг/м 3 .
Теплопроводность, плотность и свойства пара бензола
Свойства пара бензола
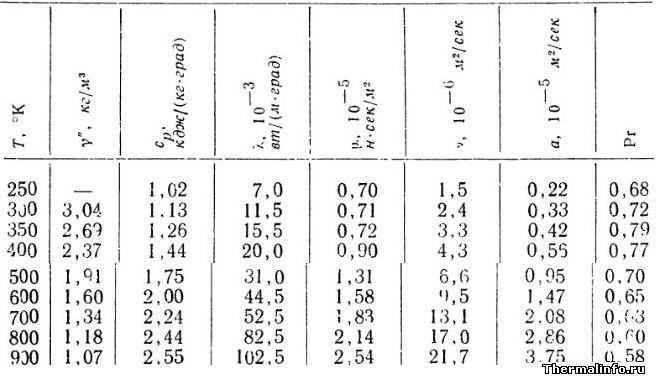
В таблице представлены теплофизические свойства пара бензола C6H6 при атмосферном давлении.
Даны значения следующих свойств: плотность, теплоемкость, коэффициент теплопроводности, динамическая и кинематическая вязкость, температуропроводность, число Прандтля в зависимости от температуры. Свойства даны в диапазоне температуры от 250 до 900 К.
По данным таблицы видно, что значения плотности и числа Прандтля при повышении температуры газообразного бензола уменьшаются. Удельная теплоемкость, теплопроводность, вязкость и температуропроводность при нагревании пара бензола увеличивают свои значения.
Следует отметить, что плотность пара бензола при температуре 300 К (27°С) составляет 3,04 кг/м 3 , что намного ниже этого показателя у жидкого бензола (см. таблицу плотности бензола и толуола).
Примечание: Будьте внимательны! Теплопроводность в таблице указана в степени 10 3 Не забудьте разделить на 1000.
Теплопроводность пара бензола
В таблице даны значения теплопроводности пара бензола при атмосферном давлении в зависимости от температуры в интервале от 325 до 450 К.
Примечание: Будьте внимательны! Теплопроводность в таблице указана в степени 10 4 . Не забудьте разделить на 10000.
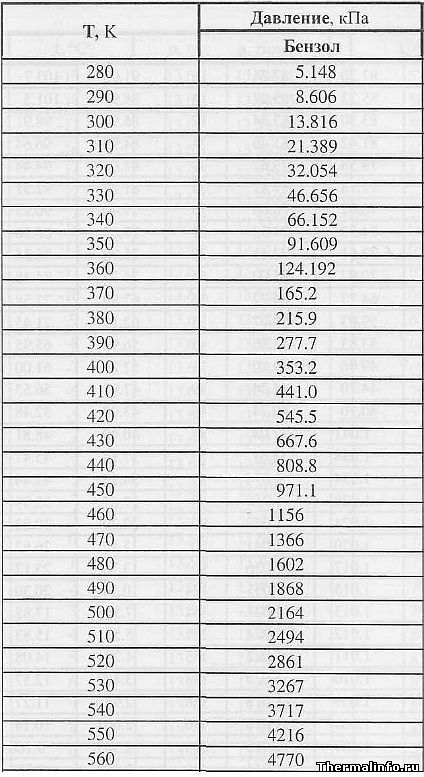
Таблица давления насыщенного пара бензола.
В таблице приведены значения давления насыщенного пара бензола в диапазоне температуры от 280 до 560 К. Очевидно, что при нагревании бензола давление его насыщенных паров увеличивается.
1. Варгафтик Н. Б. Справочник по теплофизическим свойствам газов и жидкостей.
2. Чиркин В. С. Теплофизические свойства материалов ядерной техники.
3. Волков А. И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
Теплопроводность, плотность и свойства пара бензола
Свойства пара бензола
В таблице представлены теплофизические свойства пара бензола C6H6 при атмосферном давлении.
Даны значения следующих свойств: плотность, теплоемкость, коэффициент теплопроводности, динамическая и кинематическая вязкость, температуропроводность, число Прандтля в зависимости от температуры. Свойства даны в диапазоне температуры от 250 до 900 К.
По данным таблицы видно, что значения плотности и числа Прандтля при повышении температуры газообразного бензола уменьшаются. Удельная теплоемкость, теплопроводность, вязкость и температуропроводность при нагревании пара бензола увеличивают свои значения.
Следует отметить, что плотность пара бензола при температуре 300 К (27°С) составляет 3,04 кг/м 3 , что намного ниже этого показателя у жидкого бензола (см. таблицу плотности бензола и толуола).
Примечание: Будьте внимательны! Теплопроводность в таблице указана в степени 10 3 Не забудьте разделить на 1000.
Теплопроводность пара бензола
В таблице даны значения теплопроводности пара бензола при атмосферном давлении в зависимости от температуры в интервале от 325 до 450 К.
Примечание: Будьте внимательны! Теплопроводность в таблице указана в степени 10 4 . Не забудьте разделить на 10000.
Таблица давления насыщенного пара бензола.
В таблице приведены значения давления насыщенного пара бензола в диапазоне температуры от 280 до 560 К. Очевидно, что при нагревании бензола давление его насыщенных паров увеличивается.

1. Варгафтик Н. Б. Справочник по теплофизическим свойствам газов и жидкостей.
2. Чиркин В. С. Теплофизические свойства материалов ядерной техники.
3. Волков А. И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
Бензол — свойства. T: +5,6/+200°C. Температуры кипения, плавления, критическая, молярная масса, плотность, вязкость, теплоемкость, теплота парообразования, теплопроводность, число Прандтля, коэффициент объемного расширения
Бензол — свойства. T: +5,6/+200°C. Температуры кипения, плавления, критическая, молярная масса, плотность, вязкость, теплоемкость, теплота парообразования, теплопроводность, число Прандтля, коэффициент объемного расширения.
Бензол (PhH, фен, фениловый водород, бензен) — C6H6, органическое химическое соединение, бесцветная жидкость со специфическим сладковатым запахом. Простейший ароматический углеводород. Бензол входит в состав бензина, широко применяется в промышленности, является исходным сырьём для производства лекарств, различных пластмасс, синтетической резины, красителей. Хотя бензол входит в состав сырой нефти, в промышленных масштабах он синтезируется из других её компонентов. Токсичен, канцерогенен.
Применение.
- Значительную часть получаемого бензола используют для синтеза других продуктов:
- около 50 % бензола превращают в этилбензол (алкилирование бензола этиленом);
- около 25 % бензола превращают в кумол (алкилирование бензола пропиленом);
- приблизительно 10-15 % бензола гидрируют в циклогексан;
- около 10 % бензола расходуют на производство нитробензола;
- 2-3 % бензола превращают в линейные алкилбензолы;
- приблизительно 1 % бензола используется для синтеза хлорбензола.
- В существенно меньших количествах бензол используют для синтеза некоторых других соединений.
- Изредка и в крайних случаях, ввиду высокой токсичности, бензол используют в качестве растворителя. Кроме того, бензол входит в состав бензина.
- В 1920-х — 1930-х годах, бензол добавлялиrude в прямогонный бензин для повышения его октанового числа, но к 1940-м годам такие смеси не выдержали конкуренции с высокооктановыми бензинами. Ввиду высокой токсичности содержание бензола в топливе ограничено современными стандартами введением до 1 %.
Бензол — свойства. T: +5,6/+200°C. Температуры кипения, плавления, критическая, молярная масса, давление насыщенных паров, плотность, вязкость динамическая, теплоемкость, удельная теплота парообразования, теплопроводность, число Прандтля, коэффициент объемного расширения. Таблица.
Источник: Справочное пособие к курсовому проектированию по процессам и аппаратам химической технологии. «Чувашский государственный университет имени И.Н. Ульянова» Химико-фармацевтический факультет ТЕПЛОФИЗИЧЕСКИЕ СВОЙСТВА ЖИДКИХ ВЕЩЕСТВ И РАСТВОРОВ / 2016